4.2.5 Názvy ligandů
Názvy aniontových ligandů (organických i anorganických) mají zakončení „–o“. Názvy nejběžnějších aniontových ligandů jsou shrnuty v tabulce X.
Tabulka X: Přehled běžně frekventovaných aniontových ligandů koordinačních částic
| ANIONTOVÝ LIGAND | ||
| vzorec | název aniontu | název ligandu |
| F– | fluorid | fluoro- |
| Cl– | chlorid | chloro- |
| Br– | bromid | bromo- |
| I– | jodid | jodo- |
| O2– | oxid | oxo- |
| HO2– | hydrogenperoxid | hydrogenperoxo- |
| O2– | hyperoxid | dioxygeno(1–) |
| O22– | peroxid | peroxo- |
| S2– | sulfid | thio- |
| S22– | disulfid | disulfido- |
| HS– | hydrogensulfid | merkapto- |
| H– | hydrid | hydrido- |
| OH– | hydroxid | hydroxo- |
| CN– | kyanid | kyano- |
| OCN– | kyanatan | kyanato- (vazba přes atom kyslíku) |
| SCN– | thiokyanatan | thiokyanato- (vazba přes atom síry) |
| NCO– | isokyanatan | isokyanato- (vazba přes atom dusíku) |
| NCS– | isothiokyanatan | isothiokyanato- (vazba přes atom dusíku) |
| NO2– | dusitan | nitro- (vazba přes atom dusíku) |
| ONO– | dusitan | nitrito- (vazba přes atom kyslíku) |
| NO3– | dusičnan | nitrato- |
| SO42– | síran | sulfato- |
| SSO32– | thiosíran | thiosulfato- |
| SO32– | siřičitan | sulfito- |
| CO32– | uhličitan | karbonato- |
| PO43– | fosforečnan | fosfato- |
| HPO42– | hydrogenfosforečnan | hydrogenfosfato- |
| H2PO4– | dihydrogenfosforečnan | dihydrogenfosfato- |
| CH3COO– | octan | acetato- |
| CH3OSOO– | methylsulfit (methylsiřičitan) | methylsulfito- |
| CH3CONH– | acetamid | acetamido- |
| (CH3)2N– | dimethylamid | dimethylamido- |
| NH2– | amid | amido- |
| NH2– | imid | imido- |
| N3– | nitrid | nitrido- |
| N3– | azid | azido- |
| CH3O– | methoxid | methoxo- |
| CH3S– | methanthiolat | methanthiolato- |
Příklady:
| Na[B(NO3)4] | tetranitratoboritan(1–) sodný |
| K2[OsCl5N)] | pentachloro-nitridoosmian(2–) draselný |
| Na3[Ag(S2O3)2] | bis(thiosulfato)stříbrnan(3–) sodný |
| [Ru(NH3)4(HSO3)2] | tetraamo-bis(hydrogensulfito)ruthenatý komplex |
| NH4[Cr(NH3)2(NCS)4] | diamo-tetrakis(isothiokyanato)chromitan(1–) amonný |
| K[AgF4] | tetrafluorostříbřitan(1–) draselný |
| Ba[BrF4]2 | tetrafluorobromitan(1–) barnatý |
| Cs[ICl4] | tetrachlorojoditan(1–) cesný |
| K[Au(OH)4] | tetrahydroxozlatitan(1–) draselný |
| K[CrF4O] | tetrafluoro-oxochromičnan(1–) draselný |
| K2[CrNH3(CN)2(O)2(O2)] | amo-dikyano-dioxo-peroxochroman(2–) draselný |
| [AsS4]3- | tetrathioarseničnanový(3–) ion |
| K2[Fe2(NO)4S2] | tetranitrosyl-dithiodiželeznan(2–) draselný |
| K[Au(S2)S] | disulfido-thiozlatitan(1–) draselný |
Názvy aniontových ligandů, jež jsou odvozeny od organických sloučenin odštěpením protonu (jiné ligandy než ty, které jsou pojmenovány v tabulce X), mají zakončení „-ato”. Názvy těchto ligandů se uvádějí v závorkách, bez ohledu na to, zda organický ligand je či není substituovaný, např. (benzoato), (p-chlorfenolato), (2-(chlormethyl)-1-naftolato).
Příklady:
| [Ni(C4H7N2O2)2] | bis(2,3-butandiondioximato)nikelnatý komplex |
| [Cu(C5H7O2)2] | bis(2,4-pentandionato)měďnatý komplex |
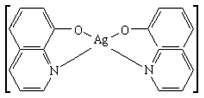 |
bis(8-chinolinato)stříbrnatý komplex |
Tvoří-li organická sloučenina ligandy s různým záporným nábojem (v důsledku ztráty různého počtu protonů), vyznačí se celkový náboj ligandu za jeho názvem pomocí Ewensova-Bassetova čísla v kulaté závorce.
Příklady:
| -OOCCH(O-)CH(OH)COO- | tartarato(3–) |
| -OOCCH(OH)CH(OH)COO- | tartarato(2–) |
Název neutrálních a kationtových ligandů se používá beze změny (mají tedy stejné pojmenování jako příslušná sloučenina, resp. kation či atomová skupina), přišemž k zápisu organických ligandů do vzorců koordinačních sloučenin se často využívá názvoslovných zkratek, diskutovaných v kapitole 4.2.7. Výjimku tvoří ligandy H2O, NH3, NO a CO (nazývají se „aqua“, „amo“, „nitrosyl“ a „karbonyl“ – viz tabulka XI). Všechny neutrální a kladně nabité ligandy (s výjimkou čtyř uvedených ligandů) se dávají v názvu sloučeniny do závorky.
Tabulka XI: Přehled běžně frekventovaných neutrálních ligandů koordinačních částic
| NEUTRÁLNÍ LIGAND | |||||
| vzorec | sloučenina | název | vzorec | sloučenina | název |
| H2O | voda | aqua- | CO | oxid uhelnatý | karbonyl- |
| NH3 | amoniak | amo- | NO | oxid dusnatý | nitrosyl- |
| O2 | molekulární kyslík | dioxygen- | O | atomový kyslík | oxygen- |
Příklady ( ligandy z tabulky XI):
| [Cr(H2O)6]Cl3 | chlorid hexaaquachromitý |
| [Co(NH3)5Cl]Cl2 | chlorid pentaamin-chlorokobaltitý |
| Na2[Fe(CN)5NO] | pentakyano-nitrosylželezitan(2–) sodný |
| K[Co(CO)2(CN)(NO)] | draselná sůl dikarbonyl-kyano-nitrosylkobaltu(1–) |
| [CoH(CO)4] | hydrido-tetrakarbonylkobaltný komplex |
Příklady (další neutrální ligandy):
| [Co(C4H8N2O2)Cl2] | bis(2,3-butandiondioxim)-dichlorokobaltnatý komplex |
| cis-[PtCl2(Et3P)2] | cis-dichloro-bis(triethylfosfin)platnatý komplex |
| [CuCl2(CH3NH2)2] | dichloro-bis(methylamin)měďnatý komplex |
| [Pt(py)4][PtCl4] | tetrachloroplatnatan tetrakis(pyridin)platnatý |
| [Fe(bpy)3]Cl2 | chlorid tris(2,2`-bipyridin)železnatý(2–) |
| [Co(en)3]2(SO4)3 | síran tris(ethylendiamin)kobaltitý(3+) |
| [Zn{NH2CH2CH(NH2)CH2NH2}2]I2 | jodid bis(1,2,3-triaminopropan)zinečnatý(2+) |
| K[PtCl3(C2H4)] | trichloro-(ethylen)platnatan(1–) draselný |
| [Cr(C6H5NC)6] | hexakis(fenylisokyanid)chrom |
| [Ru(NH3)5(N2)]Cl2 | chlorid pentaamo-(dinitrogen)ruthenatý(2+) |
Příklad (kationtové ligandy):
| [PtCl2{N(CH3)4}]Cl | chlorid dichloro-(tetramethylamonium)platnatý(1+) |
| [PtCl2{H2NCH2CH(NH2)CH2NH3)}]Cl | chlorid dichloro-(2,3-diaminopropylamonium)platnatý(1+) |
PdF, Pedagogická fakulta, Masarykova univerzita
Návrat na úvodní stránku webu, nahoru
Technická spolupráce:
Servisní středisko pro e-learning na MU
Fakulta informatiky Masarykovy univerzity, 2009
